Согласно данным научных исследований, при введении экзогенных ферментов в корм усваивается в среднем 25–35% их исходного количества, что указывает на частичную деградацию под воздействием пищеварительных процессов.
Физиология ЖКТ
Пищеварение у моногастричных животных включает четыре ключевых этапа. Первый этап происходит в ротовой полости: здесь механическое измельчение корма, смачивание слюной и обработка эндогенной амилазой обеспечивают начальную обработку пищи (Arkhipovets, 1962). Этот процесс не оказывает значительного влияния на активность экзогенных ферментов.
На втором этапе корм попадает в желудок, где сталкивается с агрессивной средой: соляная кислота (HCl) вызывает денатурацию белков, а пепсин инициирует их протеолитическое расщепление. Эти факторы могут снижать стабильность и активность добавленных ферментов.
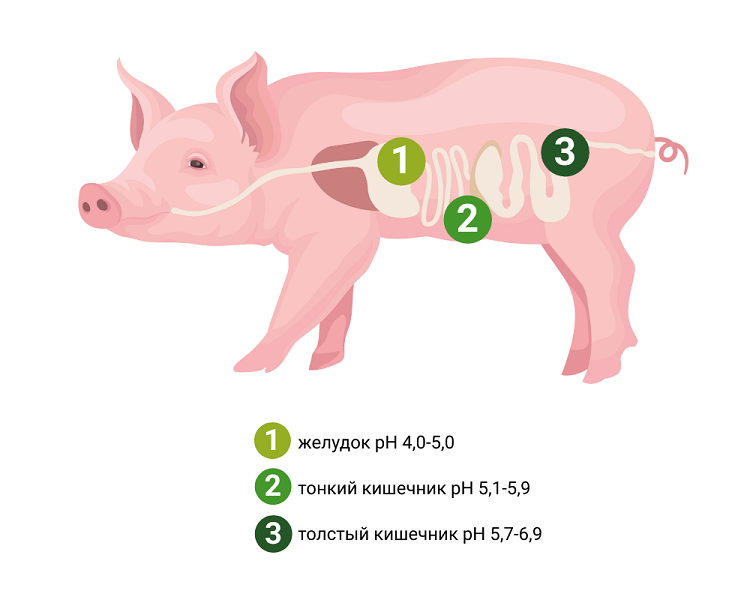

Третий этап протекает в тонком кишечнике. Здесь пищевой комок нейтрализуется щелочным секретом поджелудочной железы, содержащим бикарбонат и пищеварительные ферменты — амилазу, липазы, протеазы (Corring, 1982). Основное переваривание и всасывание питательных веществ, включая сахара, жиры, аминокислоты и минералы, происходит именно в этом отделе. Однако экзогенные ферменты, будучи белками, также подвергаются расщеплению в ходе естественных пищеварительных процессов.
На заключительном этапе пищевой комок поступает в толстый кишечник. Здесь микрофлора инактивирует остаточные эндогенные ферменты и завершает переваривание труднорастворимых компонентов — некрахмалистых полисахаридов (НПС / NSP) и белков (Gibson et al., 1989).
Время нахождения в отделах ЖКТ
Время нахождения экзогенных ферментов в отделах ЖКТ играет ключевую роль, так как в каждом сегменте существуют специфические условия, угрожающие их активности. Это время имеет двойственную роль. С одной стороны, ферментам необходим продолжительный контакт с субстратом для эффективного расщепления. Например, разрушение некрахмалистых полисахаридов занимает несколько часов (Rasmussen and Meyer, 2010; Rasmussen et al., 2012), а полное дефосфорилирование фитиновой кислоты также требует длительного периода активности (Bohn et al., 2007). С другой стороны, длительное воздействие агрессивных факторов — низкого pH и протеолитических ферментов — приводит к денатурации и расщеплению молекул, снижению их каталитической активности.
Большинство экзогенных ферментов проявляют активность только в нейтральной или слабокислой среде, поэтому в кислой среде желудка их способность расщеплять субстраты минимальна. Время пребывания в желудке критично для сохранения их функциональности. В пищеварительном тракте птиц корм перемещается быстро: среднее время удержания в отделах, кроме подвздошной кишки, составляет около 3–4 часов (Svihus, 2011). Ферменты взаимодействуют с пищей крайне ограниченное время — в передних отделах ЖКТ корм находится всего 60–90 минут.
У взрослых свиней время удерживания в желудке варьируется от 1 часа (независимо от содержания клетчатки в рационе) до 13 часов при высоковолокнистых и водоудерживающих диетах (van Leeuwen et al., 2007; Wilfart et al., 2007). Большая вариация во времени удержания корма связана с тем, что снижение частоты кормления приводит к увеличению времени удерживания в желудке, так как животные потребляют большие порции. В другом исследовании 50% корма проходили желудок через 3 или 5 часов после небольшой или крупной порции соответственно (Gregory et al., 2007).
Время пребывания в тонком кишечнике составляет от 4 часов (при частом кормлении, Wilfart et al., 2007) до 21 часа (при высоковолокнистой диете, van Leeuwen et al., 2007).
Кислотность
Корм для животных обычно имеет нейтральный pH, тогда как в пищеварительном тракте птиц и животных среда кислая в желудке (или зобе) и слабокислая в средней части кишечника. В конечной части кишечника pH сдвигается к нейтральным или слабощелочным значениям.
Оптимальный диапазон pH для активности экзогенных ферментов — 4–6 (Svihus, 2011). Однако эффективность разных ферментов варьируется: одни проявляют активность при более низких значениях pH, другие — при повышенных. Экзогенные ферменты, как правило, начинают действовать в передних отделах ЖКТ (зоб, желудок), расщепляя субстраты до того, как их обработают эндогенные ферменты (Selle and Ravindran, 2007).
Устойчивость к пепсину — ключевой фактор для сохранения активности. Например, ферменты, стабильные в кислой среде (фитазы E. Coli) не разрушаются под действием пепсина и ферментов поджелудочной железы (Igbasan et al., 2000). Это позволяет им сохранять каталитические свойства в желудке и тонком кишечнике.
В желудке уровень pH варьируется, что делает его ключевым фактором, определяющим активность и устойчивость ферментов. Несмотря на устоявшееся мнение о крайне низком pH, его значения колеблются от 1 до 5. Это связано с буферным эффектом, возникающим при поступлении корма (Iraki et al., 1997; Karamanolis et al., 2008). Исследования показывают, что при кормлении кукурузой pH желудка обычно превышает 4,0, но ночью снижается до 2,5, а при отсутствии корма — до 2,1 (Ange et al., 2000).
При скармливании ячменя pH желудка повышается до 5,0, однако спустя 7,5 часов он опускается ниже 3,0 независимо от добавления отрубей или овса (Potkins et al., 2007). В другом эксперименте с ячменным рационом pH химуса в двенадцатиперстной кишке свиней снизился с 4,8 до 4,0 в течение 4 часов (Baas and Thacker, 1996).
В тонком кишечнике pH повышается благодаря бикарбонатному секрету поджелудочной железы. У кур pH в терминальном отделе подвздошной кишки стабилен (5,7–6,0) даже при рационах с высоким содержанием клетчатки или органических кислот (Partanen et al., 2007).
Эндогенные протеазы
Желудочно-кишечный тракт свиньи секретирует несколько протеаз, включая пепсин, трипсин и химотрипсин. Эти ферменты играют ключевую роль в переваривании белков, что делает их основным препятствием для эффективного использования экзогенных ферментов. Для прогнозирования активности добавок в реальных условиях критически важно оценивать их устойчивость к протеолизу (Strube et al., 2013).
Эксперименты in vitro подразумевают инкубацию экзогенных ферментов с эндогенными протеазами. Обычно их смешивают в соотношении 0,001–0,1 (пепсин или трипсин к кормовым ферментам) на протяжении 2 часов (Pandee et al., 2011; Rodriguez et al., 1999, 2000). На активность экзогенных ферментов также влияет протеолитическая среда желудка и тонкого кишечника, где доминируют трипсин и другие кишечные ферменты.
Содержание воды и ионные связи
Активность ферментов зависит от ионной силы среды (содержания в ней ионов и их силы заряда): их функциональность ограничена при низких концентрациях солей, достигает пика в определенных условиях и снижается при избытке. Например, грибковая пектиназа проявляет максимальную активность при 0,1 М NaCl (Dahodwala et al., 1974), а глюканаза — при 0,2 М NaCl (Sena et al., 2011). Галофильные ферменты, напротив, требуют высоких концентраций солей (5–15 % NaCl) для оптимальной работы (Wainø and Ingvorsen, 2003).
Для активации ферментов необходима водная среда. При скармливании корма с экзогенными ферментами увлажнение происходит постепенно: корм набухает, продвигаясь по ЖКТ (Svihus, 2011). В тонком кишечнике ионные условия более благоприятны для стабильности ферментов, чем в желудке. Низкое содержание воды в желудке повышает вязкость среды, что снижает активность ферментов (Uribe and Sampedro, 2003). В тонком кишечнике, где вода доступнее, их эффективность возрастает.
Анализ активности ферментов
Ферменты представляют собой продукты биологического происхождения, катализирующие биохимические реакции, которые играют ключевую роль в жизнедеятельности клетки. Это белки с высокой молекулярной массой, находящейся в диапазоне от 10 000 до 500 000 дальтонов, способные осаждаться под воздействием спирта, ацетона и сульфата аммония. Подобно другим белкам, ферменты проявляют чувствительность к изменениям физико-химических условий среды, что может приводить к изменению их активности. Их функциональность основана исключительно на каталитическом действии, в отличие от других кормовых добавок, таких как витамины, стимуляторы роста или аминокислоты, чья эффективность обусловлена метаболическими процессами. Ферменты способны катализировать реакцию большого количества вещества, называемого субстратом, за короткий промежуток времени. Согласно документальным данным, один моль фермента может взаимодействовать с субстратом от 1000 до 10000 раз в секунду, при этом сам катализатор остается химически неизменным по завершении реакции. Высокая скорость ферментативных реакций объясняется значительным сродством фермента к субстрату, которое проявляется в образовании связи между ними и последующем высвобождении преобразованного продукта.
Фермент специфичен для субстрата и катализирует строго определенную реакцию в заданных условиях. В отличие от биохимических катализаторов, химические катализаторы воздействуют на более широкий спектр компонентов. Химические реакции часто носят неспецифический характер, а их избирательность достигается за счет подбора реактивов и их концентрации. Фермент же проявляет специфичность к конкретной реакции на определенном субстрате: целлюлаза взаимодействует с целлюлозой, глюканаза — с глюканами, ксиланаза — с арабиноксиланом, амилаза — с крахмалом, протеиназа — с белками, сохраняя активность даже в присутствии других реагентов. Кроме того, для эффективного взаимодействия требуется субстрат определенного качества. Ксиланаза, например, демонстрирует схожие результаты при работе с ксилановыми субстратами, выделенными из древесины березы или пшеницы, что подтверждает зависимость активности фермента от структурных особенностей мишени.
Взаимодействие между ферментом, субстратом и продуктами реакции чувствительно к физико-химическим условиям, способным изменять скорость процесса. Каталитическое действие в конкретных условиях возможно исключительно при связывании фермента с субстратом, которое зависит от конформации белка, регулируемой рН и температурой. Эти параметры напрямую влияют на реакционную способность. Например, активность эндо-1,3(4)-β-глюканазы из Penicillium funiculosum различается при измерении при рН 3 или 5, а также при температурах 40°C или 60°C. Это подчеркивает необходимость строгого соблюдения условий, указанных производителем, при оценке активности ферментов. Учет параметров анализа (рН, температура, концентрация) критичен при интерпретации результатов, особенно при сравнении ферментов из разных источников. Кривые активности, полученные в контролируемых условиях in vitro, не всегда отражают реальные процессы in vivo, где на активность влияют дополнительные факторы: ионная сила, химическая среда, концентрация и качество субстрата. Сложность соотнесения in vitro-активности с зоотехнической эффективностью обусловлена тем, что последняя зависит от трансформации кормовых компонентов в пищеварительной системе животных.
Активность фермента характеризуется скоростью превращения субстрата, определяемой как количество преобразованного вещества или образовавшегося продукта в единицу времени. Для измерения этой величины в анализе создают избыток субстрата, чтобы минимизировать изменения условий реакции, и регистрируют количество прореагировавшего субстрата или накопившегося продукта за секунду. Результат выражают в единицах активности, отнесенных к единице массы или объема препарата. Условия реакции стандартизируют, так как скорость процесса прямо пропорциональна количеству фермента в заданных пределах, что обеспечивает сопоставимость данных.
Единицы ферментативной активности определяются через количественные показатели реакции в строго заданных условиях. Так, для фитазы единица активности соответствует количеству фермента, высвобождающему 1 нмоль неорганического фосфата из фитата натрия за 1 минуту. Для эндо-1,3(4)-β-глюканазы аналогичная единица отражает выход 1 мг эквивалентов мальтозы из ячменного β-глюкана за ту же временную единицу. В случае эндо-1,4-β-L-ксиланазы измерение базируется на высвобождении 1 мг эквивалентов мальтозы из ксилана березовой древесины в течение минуты. Каждое определение подразумевает стандартизацию условий анализа, что гарантирует сравнимость результатов.
Сравнимость результатов определения ферментной активности затруднена из-за отсутствия единых стандартизированных методов. Производители коммерческих ферментных добавок часто используют собственные уникальные методики для оценки активности своих продуктов. Это создает серьезную проблему: результаты, полученные разными методами, плохо сопоставимы между собой, что снижает анализируемость данных и достоверность сравнений.
В Российской Федерации ситуация частично регулируется: для ключевого фермента — фитазы — активно применяется единый ГОСТ 31487-2012. Кроме того, постепенно внедряются государственные стандарты и для определения активности ферментов, расщепляющих некрахмалистые полисахариды (НПС) (ГОСТ 31488-2012, ГОСТ Р 54905-2012 и другие).
Однако для подавляющего большинства других ферментных активностей обязательные стандарты до сих пор отсутствуют. Именно этот пробел в регулировании остается главной причиной низкой воспроизводимости и несопоставимости результатов измерений активности в отрасли.
Определение физико-химических условий анализа критически важно для корректной оценки активности ферментов. Поскольку параметры реакции (рН, температура, ионная сила) зависят от источника фермента, прямое сравнение единиц активности, измеренных в разных системах, некорректно. Активность оценивают различными методами, где ключевую роль играет качество субстрата. Для анализа эндоактивности, направленной на разрушение полимерных цепей некрахмальных полисахаридов (NSP), применяют колориметрические и вискозиметрические подходы. Эти методы фиксируют деполимеризацию NSP — ключевой эффект, определяющий эффективность ферментов в кормопроизводстве. Колориметрия оценивает концентрацию продуктов реакции через изменение оптической плотности, а вискозиметрия — через снижение вязкости субстрата, что позволяет количественно охарактеризовать расщепление макромолекул. Каждый метод требует стандартизации условий и субстрата для обеспечения воспроизводимости результатов.
Одним из подходов к оценке активности ферментов является метод, основанный на количественном определении восстанавливающих сахаров, высвобождающихся из некрахмальных полисахаридов (например, ячменного β-глюкана или карбоксиметилцеллюлозы) в ходе ферментативной реакции. Результаты выражаются через скорость реакции — количество микромолей (мкмоль) или миллиграммов (мг) восстанавливающих сахаров, образующихся в единицу времени. Однако применение этого метода в сложных матрицах, таких как корма, осложняется интерференцией со стороны других ферментов (например, целлобиогидролаз или β-глюкозидаз), которые могут частично гидролизовать субстраты и тем самым искажать показатели активности. Дополнительные погрешности возникают из-за наличия в образцах минералов или восстанавливающих веществ, приводящих к ложноповышенным результатам. Таким образом, данные методы малопригодны для анализа ферментов в кормах, если их результаты не коррелируют с данными других тестов, учитывающих подобные помехи.
Достоверная научная оценка эндоактивности ферментов в животноводстве требует методов, максимально исключающих влияние внешних факторов. Оптимальным подходом здесь является использование специализированных синтетических субстратов или методик, отслеживающих физико-химические изменения среды напрямую, а не концентрацию конечных продуктов. Яркий пример — применение субстратов, меченных хромофорами (красителями). Эти соединения химически имитируют природные молекулы-мишени. При расщеплении ферментом хромофор высвобождается, и измерение его концентрации (интенсивности сигнала) напрямую и пропорционально отражает эндоактивность. Главное преимущество этого метода — возможность стандартизации условий анализа и минимизация помех от компонентов среды, что обеспечивает высокую точность измерений в контролируемых условиях.
Однако, для практического животноводства ключевым критерием эффективности ферментных добавок остается их реальное влияние на основные продуктивные показатели в условиях конкретного хозяйства. Лабораторная оценка эндоактивности, хотя и точна, является сложно осуществимой и экономически нецелесообразной; окончательное суждение об их полезности формируется по результатам производственных испытаний (привесы, конверсия корма, сохранность и т.д.).
Единица активности фермента — это конкретное количество фермента, которое нужно, чтобы гидролизовать субстрат. В результате этого расщепления должны образоваться растворимые более короткие молекулы (олигомеры), и это должно произойти за строго заданное время в точно определенных условиях. Олигомеры поглощают свет таким образом, что при измерении на специальном спектрофотометре на определенной длине волны дают всегда одно и то же значение оптической плотности (OD). OD показывает, насколько сильно раствор поглощает свет на этой длине волны.
Главная трудность таких методов измерения активности связана с качеством самого субстрата. Субстрат — это обычно природный экстракт, к молекулам которого химически прикреплены специальные хромофорные молекулы (молекулы, которые поглощают свет и позволяют измерять OD). Проблема в том, что разные партии этого природного субстрата могут сильно отличаться по своей структуре. Это значит, что в них может быть разная степень полимеризации, разная разветвленность и другие параметры. Эта изменчивость между партиями делает очень сложным стандартизацию содержания хромофора в субстрате. Поэтому, когда начинают использовать новую партию субстрата, обязательно нужно провести калибровку измерительной шкалы. Для калибровки используют эталонный фермент — фермент с точно известной и проверенной активностью.
Методы, использующие субстраты с прикрепленными светопоглощающими хромофорами, обладают важным преимуществом: они устойчивы к помехам. Это значит, что на их результаты измерения активности фермента меньше влияют побочные реакции или наличие восстанавливающих веществ в исследуемом растворе.
Похожим образом работают вискозиметрические методы. Эти методы оценивают активность фермента по тому, насколько он снижает вязкость раствора природного субстрата. Измерения проводятся при строго контролируемых условиях pH и температуры. Точность этих вискозиметрических методов также сильно зависит от качества субстрата, особенно от его начальной вязкости. Эта начальная вязкость может меняться от партии к партии именно из-за тех же структурных особенностей (полимеризация, разветвленность), о которых говорилось раньше.
Несмотря на то, что эти методы (и хромогенные, и вискозиметрические) очень важны и хорошо подходят для анализа кормов, у них есть недостаток: они требуют множества измерений. Хотя этот процесс можно автоматизировать.
Сравнение вискозиметрических и колориметрических методов с подходами, основанными на измерении восстанавливающих сахаров, показывает их преимущество в условиях сложных матриц, например, кормов. Однако все методы остаются зависимыми от характеристик субстрата. Как следствие, один и тот же ферментный препарат может демонстрировать разные количественные результаты в зависимости от применяемого метода. Важно отметить, что числовые различия в единицах активности не отражают реальной эффективности фермента в корме.
Критика данных методов связана с использованием синтетических или модельных субстратов, не всегда соответствующих компонентам реальных кормов. Это особенно актуально для хромогенных субстратов, которые лишь имитируют природные молекулы. Кроме того, аналитические протоколы (буферные системы, рН, температура, длительность реакции) могут существенно различаться даже при одинаковом принципе измерения, что обусловлено особенностями происхождения ферментов. Примером служат рекомендации производителей по анализу ксиланаз в кормах, где наблюдается значительный разброс параметров — от выбора буфера до времени инкубации. Это подчеркивает необходимость унификации условий для сопоставимости результатов.
Методы анализа ферментативной активности тесно связаны с происхождением продукта, а использование разных субстратов и подходов может приводить к расхождению результатов. Основные методологические сложности возникают из-за необходимости стандартизации экспериментальных условий и обеспечения качества субстрата. Производители ферментов разрабатывают специализированные методы анализа для каждого типа фермента, поскольку надежные протоколы критически важны для контроля качества продукции. Однако создание универсального стандарта для измерения активности невозможно: даже ферменты с одинаковым молекулярным механизмом действия требуют разных условий анализа (рН, температура). Для фермента конкретного происхождения оптимальные результаты достигаются при использовании одного или нескольких методов, адаптированных к его специфическим характеристикам.
Анализ активности ферментов в кормах сопряжен с дополнительными сложностями. Корм может содержать эндогенные ферменты, которые искажают результаты, а также компоненты, мешающие измерениям (например, продукты разложения или вещества, образующиеся при производстве корма). Вариабельность рецептур, качества сырья и условий обработки усиливает риск погрешностей. Целлюлолитические ферменты, способные связываться с компонентами корма, часто требуют эффективных методов экстракции для точного определения активности. Эти факторы делают выбор метода анализа и контроль условий ключевыми аспектами достоверной оценки ферментных препаратов в реальных применениях.
На основе представленных данных можно сформулировать следующие выводы:
- Применение ферментов в кормопроизводстве требует решения ключевых задач, среди которых приоритетными являются выбор подходящего препарата и контроль его дозировки в рационе.
- Для каждой ферментативной активности, полученной из конкретного микроорганизма, производитель предлагает специализированные методы анализа. Однако при адаптации этих методов к измерению активности в кормах необходимо учитывать особенности матрицы, включая состав и возможные компоненты, влияющие на активность ферментов.
- Оценка ферментов исключительно по количеству единиц активности недостаточна для принятия решений, поскольку их числовые значения зависят от источника фермента и применяемой методики анализа, что снижает их сравнительную значимость.
- Единственным объективным способом оценки эффективности ферментов в реальных условиях, помимо тестирования стабильности, остаются in vivo -исследования, отражающие взаимодействие препарата с организмом животного и его влияние на продуктивность.
Термостабильность
Стабильность ферментов является решающим фактором, определяющим коммерческий успех их применения. Ферменты частично теряют свою активность под действием тепла, экстремальных значений рН или протеаз.
С повышением температуры увеличивается скорость ферментативных реакций. Повышение температуры на десять градусов по Цельсию увеличивает активность большинства ферментов на 50–100% (правило Вант-Гоффа). Однако это увеличение происходит только до определенного порога денатурации, когда повышенная температура нарушает третичную структуру белка, что приводит к потере его каталитической функции. После денатурации фермент не может быть восстановлен. Поскольку каждый фермент уникален по структуре и типу стабилизирующих связей (водородных, ионных, гидрофобных), температура денатурации специфична для каждого типа фермента. Так, большинство ферментов животного происхождения денатурируются выше 40°C.
Важно понимать, что температура отражает кинетическую энергию молекул в системе. При ее повышении увеличивается частота столкновений между ферментом и субстратом, и больше молекул достигает энергии активации, что ускоряет реакцию — но только до достижения температурного оптимума. Избыточная кинетическая энергия разрывает слабые связи (водородные, дисульфидные, гидрофобные взаимодействия), стабилизирующие третичную структуру фермента, вызывая термическую денатурацию и потерю активности. При этом большинство субстратов (например, глюкоза или кислород) устойчивы к нагреву, и основным ограничивающим фактором является стабильность самого фермента. Ферменты постепенно теряют активность даже при умеренных температурах из-за спонтанной деградации или окисления. Хранение при +5°C или ниже замедляет эти процессы. Хотя низкие температуры снижают активность ферментов, это состояние обычно обратимо: при нагреве каталитическая функция восстанавливается. Однако многократное замораживание и оттаивание или формирование кристаллов льда может необратимо повредить белок.
Температурный оптимум — это диапазон, в котором скорость ферментативной реакции максимальна. Он значительно варьируется в зависимости от происхождения фермента. Оптимум около 37°C характерен для ферментов мезофильных организмов, таких как человек или сельскохозяйственные животные. Верхний предел активности определяется температурой денатурации конкретного белка, а не фиксированным значением. Для повышения стабильности ферментов в промышленности используют иммобилизацию на полимерных носителях, инженерную модификацию (направленную эволюцию, стабилизацию активного центра) или добавление защитных веществ (полиолов, кофакторов). Кислотно-щелочная стабильность (pH-стабильность) зависит от заряда аминокислот в активном центре, а устойчивость к протеазам связана со степенью структурированности поверхности белковой молекулы. Все эти факторы критически влияют на эффективность и экономическую целесообразность использования ферментов в биотехнологиях.
Применение термостабильных ферментов в кормах для животных имеет решающее значение из-за высокотемпературных процессов, используемых при их производстве, в первую очередь гранулирования или экструзии. В процессе гранулирования кормовые смеси подвергаются воздействию пара и механического давления при температурах от 70°C до 90°C (а иногда и выше) для формирования прочных гранул. Обычные ферменты быстро денатурируют (теряют свою структуру и функцию) под воздействием такого интенсивного тепла, становясь неактивными еще до того, как корм попадет к животному. Термостабильные же ферменты сохраняют свою биологическую активность после такой термической обработки, гарантируя, что они останутся неповрежденными и функциональными в конечном кормовом продукте.
Помимо выживания при гранулировании, термостабильность также повышает стабильность фермента при хранении корма и его функциональную устойчивость в пищеварительном тракте животного. Хотя температуры пищеварения (около 40°C у свиней, 41–42°C у птицы) ниже температур гранулирования, термостабильные ферменты часто демонстрируют превосходную стабильность в различных диапазонах pH и устойчивость к протеолитическому расщеплению в кишечнике. Такая стабильность обеспечивает более последовательную и продолжительную ферментативную активность во время пищеварения, улучшая расщепление антипитательных факторов и повышая усвоение питательных веществ.
Без термостабильных ферментов производителям кормов пришлось бы добавлять ферменты после гранулирования (например, путем жидкого покрытия), что усложняет процесс, увеличивает затраты и несет риск неравномерного распределения.
Как выбрать фермент?
Кормовые ферменты должны соответствовать нескольким ключевым критериям:
- сохранять высокую специфическую активность в условиях пищеварительного тракта целевых животных (то есть работать при определенных pH, температуре и в присутствии других пищеварительных соков),
- выдерживать термическую обработку корма (во избежание денатурации при гранулировании или экструзии),
- не повышать существенно стоимость кормов,
- оставаться стабильными при длительном хранении,
- а также быть безопасными для животных и человека.
Выбор оптимальных ферментов зависит от множества взаимосвязанных факторов: вида, возраста, физиологического состояния и даже породы животных, а также типа и состава кормового сырья (включая уровень антипитательных факторов). Эффективность ферментов варьируется в зависимости от этих параметров, что требует тщательного научного обоснования и подбора дозировок для конкретного применения. Так, действие одних и тех же ферментов может существенно различаться у свиней и птицы из-за особенностей их пищеварения или при использовании ячменя вместо пшеницы из-за разного содержания и структуры клетчатки или ингибиторов. Поэтому ключевым этапом является проведение исследований эффективности (in vitro и in vivo) и оценка влияния ферментов на зоотехнические показатели (привесы, конверсию корма) и здоровье животных в конкретных условиях применения. Так же крайне важно отметить необходимость использования стандартизированных методов оценки активности ферментов производителем (ГОСТ). Такие данные позволят более корректно оценить эффективность и целесообразность применения тех или иных ферментов без необходимости проведения дорогостоящего производственного испытания.
Заключение
Эффективность экзогенных ферментов в кормах для животных, направленных на улучшение усвоения питательных веществ и повышение продуктивности, подтверждена многочисленными исследованиями. Однако их потенциал ограничен физиологическими особенностями ЖКТ, такими как кислотность среды, время удержания пищевой массы и взаимодействие с эндогенными ферментами. Для максимизации эффекта от ферментных препаратов требуется комплексный подход, включающий оптимизацию рационов.
При этом важно, что активность ферментов зависит от их происхождения, условий анализа (рН, температура) и качества субстратов, которые часто отличаются по структуре — например, по степени полимеризации или разветвленности. Это приводит к вариабельности результатов даже для одного и того же препарата. Только эксперименты на животных позволяют оценить реальную эффективность препаратов.
Ферментные добавки линейки Мисма — Фит (источник фитаз), Зим G (глюканазы), Зим X (ксиланазы), Зим А (амилазы), Зим М (маннаназы), Зим П (протеазы) и Зим Мульти (комплекс глюканазы, целлюлазы и ксиланазы) — демонстрируют высокую эффективность в условиях in vitro и in vivo. Их стабильные результаты подтверждены многолетней практикой применения на российском рынке: первый препарат линейки был официально зарегистрирован в 2016 году, а сегодня продукция зарекомендовала себя как надежное решение для сельскохозяйственных предприятий.
Учитывая важность синергетического действия ферментов, нами разработана специализированная линейка Мисма Зим Комби. Ее уникальность заключается в персонализированном подборе ферментных комбинаций, адаптированных под конкретные условия эксплуатации — от типа корма до особенностей технологического процесса в каждом хозяйстве. Такой подход позволяет достичь максимальной биокаталитической активности и повысить экономическую эффективность кормления.
Ключевым преимуществом линейки является строгий контроль качества: все добавки проходят тестирование по стандартизированным методикам в аккредитованной лаборатории, что гарантирует точность дозировки, стабильность активности и соответствие государственным стандартам. Это обеспечивает прозрачность результатов для производителей и позволяет с уверенностью планировать показатели продуктивности животных.
Статья подготовлена техническим отделом Мисма, август 2025.
Перепечатка и частичное использование материала только с письменного разрешения компании МИСМА.





